化学实验 · 二 · 「实验过程」
实验基本过程
实验前:①仪器选择与组装;②仪器的检验;③通入气体;④试剂的填装;⑤点火
实验后:①先移走液面内部导管(防止倒吸液体进入装置); ②关闭热源,停止反应; ③再停止通气(最后停止通气的常考目的:防止产物与空气接触) ④仪器的洗涤
五个考察点
- 仪器选择与组装:①仪器规格选择、②仪器组装
- 仪器的检验:①检验是否漏水、②气密性检验
- 通入气体:①通气到何时停止、②通气的作用
- 试剂的填装:①试剂的取用、②试剂的存放
- 仪器的洗涤:①洗涤方法、②洗涤完成标志、③常见洗涤方法
仪器选择和组装
仪器规格的选择
各类瓶瓶罐罐中液体体积范围:
- 仪器不需加热时:占容积的
- 仪器需要加热时:占容积的
- 仪器不需加热时:占容积的
量筒量取一定量的液体:应选取略大于所需液体体积的量筒。
仪器的组装
仪器组装:方向为“先下后上,从左到右”
模块化装置的安装放在第三节
仪器的检验
检验是否漏水(检漏)
检漏方法:向分液漏斗中加入少量水,检查旋塞处是否漏水; 将漏斗倒转过来,检查玻璃塞是否漏水
(补充:在玻璃旋塞两端涂一薄层凡士林,插入塞窝转动,使之均匀,以防漏水)
气密性检验
无论采用哪种装置制取气体.在成套装置组装完毕、装入反应物之前,必须检验装置的气密性,以确保实验的顺利进行。装置气密性的检验,其原理通常是设法造成装置的不同部位有压强差,并产生某种明显的现象。在叙述上要注意细节描述的严密性
步骤 具体方法 Step1:形成密闭/封闭的体系
(活塞、弹簧夹、液封)关闭:止水夹夹住导管/关闭活塞;液封:导管末端浸入水中,加水至浸没导管 Step2:①制造压强差;②描述产生的现象 ①微热法:用手焐热/酒精灯微热现象:加热气泡冒出,停止后倒吸水柱
②注水法:向漏斗注水现象:形成液柱不动/液滴无法滴下Step3:一段时间后,现象保持不变 ——
通入气体
通气到什么时候为止
- 水面下的导管,产生稳定气泡时;
- xx 装置中充满 xx 气体(描述气体颜色特点)
通气的作用:本质是各种方式去“赶跑”装置内原有气体
阶段 通气作用 实验前 排除装置中的空气,以免与空气中的 xx 发生反应( ) 实验中 ①减小气体浓度,防止出现倒吸现象(特别是极易溶于水的气体)
②将 xx 气体充分排净/将气体赶入 xx 装置
③提供惰性气体环境,防止反应物与空气反应
④减少定量实验误差
⑤增大压强,加快反应速率实验后 将气体全部吹入 xx 中充分吸收
①防止残留装置中造成污染
②减小定量实验的误差
填装物质
试剂取用
| 固体药物 | 液体药物 | |||||
|---|---|---|---|---|---|---|
| 药瓶取用 | 粉末 | 块状 | 定量 | 少量滴加 | 定量 | 大量倾倒 |
| 使用仪器 | 药匙 | 镊子 | 托盘天平 | 胶头滴管 | 量筒或滴定管 | 直接倾倒 |
| 注意事项 | 固体加入试管时:一横二放三慢竖 | 竖直悬滴 | 倾倒口对口 标签对手心 | |||
试剂存放
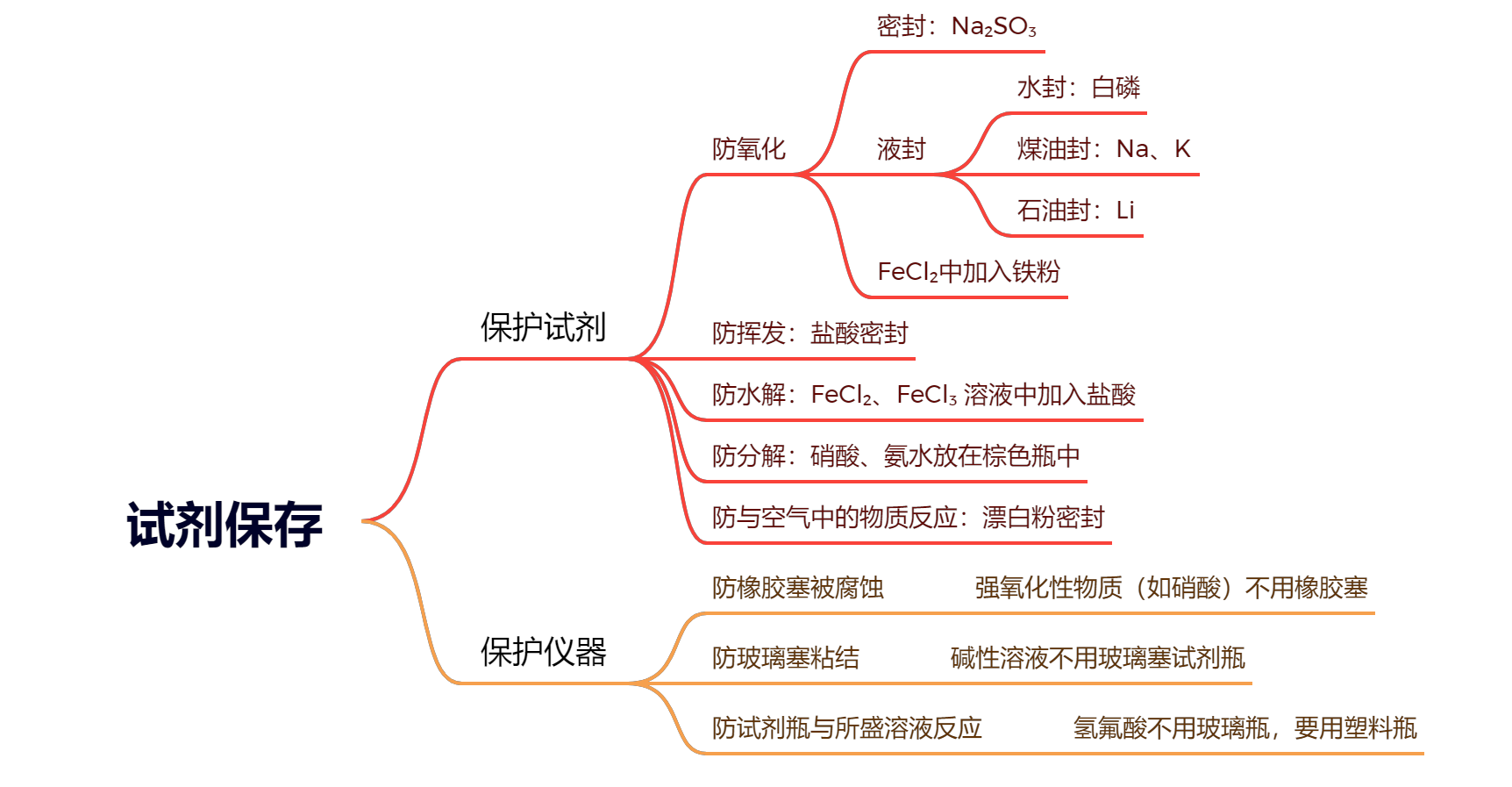
仪器洗涤
基本方法:
- 注入少量水振荡倒掉,冲洗外壁
- 若仍有污迹,用洗涤液处理后刷洗(洗涤液)
- 最后用蒸馏水冲洗。(滴定管还要润洗)
洗净的标准:内壁附着一层均匀的水膜,既不聚成水滴,也不成股流下
常考污渍的洗涤方法
附着杂质 油污 银镜 硫磺、碘、磷 乙酸乙酯 选择试剂 碱液 硝酸 (水解)或 酒精(互溶)